Sinh học phân tử, lĩnh vực nghiên cứu quan trọng về các đại phân tử và giải pháp xét nghiệm tạo bước tiến lớn trong y học
Sinh học phân tử nghiên cứu các đại phân tử (ADN, ARN, Protein) và cơ chế hoạt động của phân tử trong sinh vật sống. Đồng thời, tìm hiểu bản chất phân tử của gen cùng cơ chế sao chép, đột biến và biểu hiện gen. Xét nghiệm sinh học phân tử là kỹ thuật xét nghiệm tân tiến, được ứng dụng rộng rãi trong y học. Nó ra đời dựa trên phương pháp khuếch đại chuỗi PCR tạo ra các phản ứng PCR. Từ đó, giúp nhận biết các yếu tố gây bệnh và đưa ra phương án điều trị hiệu quả.
Nội dung
- 1 1. Sinh học phân tử là gì?
- 2 2. Ý nghĩa của nghiên cứu sinh học phân tử
- 3 3. Sinh học phân tử hiện đại
- 4 4. Quan hệ với các phân ngành sinh học khác
- 5 5. Các kỹ thuật trong sinh học phân tử
- 6 6. Mối quan hệ phức tạp của gen và protein
- 7 7. Xét nghiệm sinh học phân tử là gì?
- 8 8. Ứng dụng xét nghiệm sinh học phân tử trong chẩn đoán HBV và HIV
- 9 9. Hạn chế của xét nghiệm
- 10 10. Ứng dụng của kỹ thuật sinh học phân tử
- 11 11. Tạm kết
1. Sinh học phân tử là gì?
Sinh học phân tử là lĩnh vực sinh học nghiên cứu cấu trúc hóa học, thành phần và tương tác của tế bào trong sinh vật. Nó bao gồm quá trình tổng hợp, biến đổi, cơ chế và tương tác phân tử (Alberts B, Johnson A, Lewis J, Morgan D, Raff M, Roberts K, Walter P (2014). Molecular Biology of the Cell, Sixth Edition. Garland Science. tr. 1–10. ISBN 978-1-317-56375-4.). Đối tượng mà lĩnh vực này tập trung hướng đến là axit nucleic (ADN, ARN) và protein. Đây là các đại phân tử cần thiết cho hoạt động sống. Sinh học phân tử xuất hiện từ những năm 1930. Đồng thời, phát triển các lĩnh vực liên quan đến Hóa sinh, Di truyền, Miễn dịch, Tế bào học và Lý sinh.
Năm 1945, “sinh học phân tử” được nhà Vật lý William Astbury sử dụng. Trong đó, cách tiếp cận đơn giản và thuận tiện nhất là sử dụng vi khuẩn và thể thực khuẩn. Tuy nhiên, chỉ đưa ra các nghiên cứu cơ bản nhất. Vào năm 1953, hai nhà khoa học trẻ Francis Crick và James Watson hình thành nên mô hình mạch xoắn kép ADN. Nó đã thay đổi toàn bộ cấu trúc ADN đã được đề xuất trước đó bởi Rosalind Franklin và Maurice Wilkins. Sau mô hình này, các nghiên cứu của hai nhà khoa học tập trung nghiên cứu DNA bên trong vi sinh vật, thực vật và động vật khác (S., Verma, P. (2004). Cell biology, genetics, molecular biology, evolution and ecology. S Chand and Company. ISBN 81-219-2442-1. OCLC 1045495545.).
2. Ý nghĩa của nghiên cứu sinh học phân tử
Không chỉ nghiên cứu phân tử và sự tương tác giữa chúng. Sinh học phân tử còn chứa tập hợp các kỹ thuật giúp tìm hiểu quá trình phân tử. Trong đó, kỹ thuật đáng chú ý nhất trong cách mạng hóa lĩnh vực này là phản ứng chuỗi polymerase năm 1983. PCR là phản ứng khuếch đại lượng nhỏ ADN và ứng dụng nhiều trong đa dạng ngành khoa học (“Polymerase Chain Reaction (PCR)”, Definitions, Qeios, ngày 26 tháng 11 năm 2019, doi:10.32388/167113, S2CID 94561339).
Luận thuyết trung tâm của sinh học phân tử cho thấy dòng thông tin chạy theo một chiều. Từ DNA đến mRNA rồi đến protein. Đây cũng là quy luật của quá trình phiên mã, dịch mã và sao chép DNA. Tuy nhiên, với một số virus mang RNA, có quá trình phiên mã ngược, tạo bản sao DNA từ RNA hệ gen.
Sinh học phân tử còn đóng vai trò quan trọng trong tìm hiểu cấu trúc, chức năng. Đặc biệt là quá trình kiểm soát nội môi trong tế bào. Tất cả đều được ứng dụng trong phát triển dược phẩm và phương pháp chẩn đoán bệnh mới. Đồng thời, hiểu rõ hơn quá trình sinh lý của tế bào. Một số nghiên cứu lâm sàng và liệu pháp y tế phát triển từ lĩnh vực này được vận dụng hiệu quả trong liệu pháp gen. Còn ứng dụng sinh học phân tử trong y học được gọi là y học phân tử.
3. Sinh học phân tử hiện đại
Vào những năm 20 của thế kỷ 21, sinh học phân tử bước vào thời kỳ hoàng kim do sự phát triển của công nghệ hiện đại. Khoa học kỹ thuật cho phép nghiên cứu quá trình sinh học ở cấp độ nguyên tử theo thời gian thực. Các nhà khoa học có thể truy cập vào kho dữ liệu trình tự DNA với mức phí tiết kiệm. Từ đó, tạo nền tảng phát triển liệu pháp chỉnh sửa gen mới ở sinh vật khác. Chưa kể, nó còn đẩy mạnh quá trình sản xuất công nghiệp các tiểu và đại phân tử. Quá trình này được thực hiện nhờ trao đổi chất ngoại sinh trong đa dạng tế bào nhân thực và nhân sơ (van Warmerdam, T. “Molecular Biology Laboratory Resource”. Yourbiohelper.com.).
Dữ liệu trình tự sinh học trở thành “tài sản” quý giá khi được ứng dụng trong nhiều lĩnh vực khoa học. Nó hứa hẹn thúc đẩy sự phát triển của các ngành công nghiệp. Đồng thời, tạo điều kiện cho các nhà khoa học nghiên cứu thông tin cần thiết trong quá trình thực nghiệm. Chưa kể, các thí nghiệm chỉnh sửa gen dùng công nghệ CRISPR-Cas9 được ứng dụng trên sinh vật mới với giá dưới 10.000 đô la. Từ đó, đẩy mạnh quá trình ứng dụng công nghệ hiện đại này trong lĩnh vực công nghiệp và y tế.
4. Quan hệ với các phân ngành sinh học khác
Sinh học phân tử, hóa sinh và di truyền học có một số điểm chung. Cụ thể, cả ba đều nghiên cứu chi tiết cách thức hoạt động của sinh vật ở cấp độ phân tử. Tuy nhiên, mỗi phân ngành lại có các ứng dụng khác nhau.
-
Sinh học phân tử
Sinh học phân tử nghiên cứu cơ sở phân tử của hiện tượng sinh học. Trong đó, tập trung đến quá trình tổng hợp, biến đổi, cơ chế và tương tác.
-
Hóa sinh
Hóa sinh nghiên cứu chất hóa học và quá trình hoạt động bên trong cơ thể. Họ tập trung chủ yếu đến cấu trúc, chức năng và vai trò của các đại phân tử. Bao gồm: protein, lipid, cacbohydrat, và axit nucleic (Berg, Jeremy (2002). Biochemistry. Tymoczko, John L.; Stryer, Lubert (ấn bản 5). New York: W.H. Freeman. ISBN 0-7167-3051-0. OCLC 48055706). Ngoài ra, nó cũng nghiên cứu tác động hóa học xảy ra do lượng chất lớn hơn như nọc độc. Các phương pháp chủ yếu dựa trên nghiên cứu hóa học hữu cơ.
-
Di truyền học
Di truyền học tìm hiểu khác biệt về mặt di truyền ảnh hưởng đến các sinh vật. Cụ thể là dự đoán đột biến, gen riêng lẻ và tương tác di truyền. Những vấn đề ảnh hưởng đến biểu hiện gen và quá trình tạo nên một kiểu hình. Nó tập trung chủ yếu đến đặc điểm di truyền và sự thay đổi trong mã di truyền tác động đến sinh vật. Việc tập trung vào khả năng di truyền tốt nhất là ở cấp độ dân số. Bởi vậy, hướng nghiên cứu này có quy mô lớn hơn nhiều sinh học phân tử.
Các lĩnh vực trên gắn bó chặt chẽ và ảnh hưởng lẫn nhau. Đặc biệt, nghiên cứu di truyền học mang đến nhiều tri thức về sinh học phân tử. Nhất là liên quan đến vai trò của ARN. Khi nghiên cứu sinh học phân tử, các phương pháp từ di truyền học và hóa sinh cũng được kết hợp. Phần lớn là nghiên cứu định lượng với các kỹ thuật khoa học máy tính trong tin sinh học và sinh học tính toán. Di truyền phân tử, nghiên cứu gen là lĩnh vực phụ nổi bật nhất của sinh học phân tử. Từ đó, mở rộng kiến thức trong một số phân ngành như sinh học tế bào hay sinh học phát triển. Ngoài ra, nó còn được ứng dụng trong sinh học tiến hóa như di truyền học quần thể và phát sinh chủng loài học.
5. Các kỹ thuật trong sinh học phân tử
5.1 Nhân bản phân tử
Nhân bản phân tử là kỹ thuật được ứng dụng trong phân lập và chuyển chuỗi ADN mong muốn vào vector plasmid. Công nghệ ADN tái tổ hợp được phát triển lần đầu vào năm 1960. Trình tự ADN mã hóa cho một protein được nhân bản bằng phản ứng chuỗi polymerase (PCR) haowcj enzyme để tạo thành plasmid. Vector plasmid bao gồm: vị trí bắt đầu sao chép, vị trí tạo dòng và marker chọn lọc. Nằm ở ngược dòng MCS là vùng gen khởi động và vị trí bắt đầu quá trình phiên mã. Nó giúp điều hòa biểu hiện gen được nhân bản.
Tiếp theo, Plasmid được đưa vào tế bào vi khuẩn hoặc động vật. Một số phương pháp được sử dụng như biến nạp (hấp thụ ADN), tiếp hợp (tiếp xúc giữa các tế bào) hoặc tải nạp (vector virus). ADN được đưa vào tế bào nhân thực như tế bào động vật bằng phương pháp vật lý hoặc hóa học. Nó được gọi là quá trình chuyển nạp. Một số kỹ thuật chuyển nạp như chuyển nạp canxi photphat, điện phân, vi tiêm hay liposome. Plasmid được tích hợp trong bộ gen giúp chuyển nạp ổn định (Alberts B, Johnson A, Lewis J, Raff M, Roberts K, Walter P. Isolating, Cloning, and Sequencing DNA (bằng tiếng Anh). Truy cập ngày 31 tháng 12 năm 2016.). Còn plasmid tồn tại độc lập với bộ gen cùng biểu hiện tạm thời gọi là chuyển nạp thoáng qua.
ADN mã hóa cho protein mong muốn nằm trong tế bào. Khi đó, protein có thể được biểu hiện và sử dụng cho đa dạng mục đích. Chẳng hạn như kiểm tra hoạt động, nghiên cứu cấu trúc, tổng hợp lượng lớn protein và nghiên cứu hoạt tính của thuốc.
5.2 Phản ứng chuỗi polymerase
Phản ứng chuỗi polymerase (PCR) là kỹ thuật sao chép DNA mang tính ứng dụng cao. Nó cho phép sao chép hoặc sửa đổi trình tự ADN cụ thể theo những cách nhất định. Trong điều kiện lý tưởng, nó có thể khuếch đại một phân tử DNA thành 1,07 tỷ phân tử chỉ trong chưa đầy 2 giờ. PCR được ứng dụng trong đa dạng lĩnh vực. Bao gồm: biểu hiện gen, phát hiện tác nhân gây bệnh, đột biến gen và đưa chúng vào DNA. Kỹ thuật PCR giúp đưa vị trí enzyme giới hạn vào đầu phân tử DNA. Hoặc kích thích đột biến base cụ thể trên DNA nhờ gây đột biến có định hướng.
PCR còn giúp xác định đoạn ADN được tìm thấy trong ADN bổ sung (cADN). PCR có nhiều biến thể, như PCR phiên mã ngược (RT-PCR). Từ đó, giúp khuếch đại ARN và cho phép đo lường chính xác số phân tử ADN hoặc ARN (“Polymerase Chain Reaction (PCR)”. National Center for Biotechnology Information. U.S. National Library of Medicine. Truy cập ngày 31 tháng 12 năm 2016.).
-
Kỹ thuật tổng hợp PCR
Kỹ thuật tổng hợp PCR giúp xác định vi khuẩn nhanh chóng. Mỗi chu trình tổng hợp thường bao gồm 20 – 35 vòng lặp. Sau mỗi vòng, DNA được nhân đôi theo hệ số mũ. Để đảm bảo kết quả chính xác, quy trình này đòi hỏi thu thập mẫu bệnh phẩm chính xác với nồng độ và điều nhiệt chính xác tại mỗi giai đoạn.
Tuy nhiên, một số sai sót xảy ra khiến phản ứng PCR diễn ra thiếu hiệu quả. Thậm chí, không cho kết quả dương tính dù người bệnh có các triệu chứng rõ ràng. Đôi khi, lây nhiễm chéo giữa các mẫu kiểm tra cũng mang lại kết quả PCR dương tính. Ngay cả khi các triệu chứng lâm sàng của người bệnh không rõ ràng.
-
Kỹ thuật Real-time PCR
Kỹ thuật Real-time PCR tương đương với kỹ thuật PCR. Nó bổ sung thiết bị ghi tín hiệu trong quá trình tổng hợp PCR. Bằng cách so sánh số vòng mẫu thử và mẫu chuẩn trong cùng một khoảng thời gian phản ứng. Nhà khoa học có thể tính được số lần mẫu thử nhiều hơn mẫu chuẩn. Đây là căn cứ để xác định nồng độ DNA của mẫu thử.
Xem thêm:
- Cảm biến sinh học – Công nghệ hiện đại với đa dạng ứng dụng
- Sinh học phân tử – Cơ sở vững chắc đột phá y học
5.3 Điện di trên gel
Điện di trên gel là kỹ thuật tách phân tử theo kích thước bằng gel agarose hoặc polyacrylamide. Đây là một trong những công cụ chính của sinh học phân tử. Nguyên tắc cơ bản là các đoạn ADN được tách ra nhờ cho dòng điện chạy qua gel. Do khung xương của ADN chứa các nhóm phosphate mang điện tích âm. ADN sẽ di chuyển qua gel agarose về phía đầu mang điện tích dương (Lee, Pei Yun; Costumbrado, John; Hsu, Chih-Yuan; Kim, Yong Hoon (ngày 20 tháng 4 năm 2012). “Agarose Gel Electrophoresis for the Separation of DNA Fragments”. Journal of Visualized Experiments (62): 3923. doi:10.3791/3923. ISSN 1940-087X. PMC 4846332. PMID 22546956.). Protein cũng được phân tách nhờ sử dụng gel SDS-PAGE. Hoặc sử dụng phương pháp điện di trên gel 2D dựa trên kích thước và điện tích.
Kỹ thuật điện di Gel được sử dụng để phân tách các đoạn ADN/ARN hoặc protein. Nó được thực hiện dựa trên sự khác biệt về khối lượng và điện tích của chúng. Nguyên lý chính của kỹ thuật là các phân tử acid nucleic hay protein mang bản chất nhất định. Do đó, khi đặt trong một môi trường có điện trường, các phân tử này sẽ bắt đầu di chuyển.
Phân tử nhỏ hơn sẽ di chuyển nhanh hơn và ngược lại. Để thực hiện kỹ thuật này, nhà khoa học thường tiến hành trên gel đặc biệt hoặc điện di trên giấy. Thông qua sử dụng chất nhuộm phù hợp, vị trí của các phân tử được xác định dễ dàng và chính xác hơn.
5.4 Phương pháp xét nghiệm Bradford
Kỹ thuật sinh học phân tử thử nghiệm Bradford cho phép định lượng nhanh chóng và chính xác phân tử protein. Nó được thực hiện nhờ đặc tính độc đáo của một loại thuốc nhuộm có tên là Coomassie Brilliant Blue G-250. Coomassie Blue chuyển từ màu nâu đỏ sang xanh lam sáng khi liên kết protein. Ở điện tích dương, cấu trúc thuốc nhuộm không ổn định, có bước sóng nền 465 nm và tạo màu nâu đỏ. Khi Coomassie Blue liên kết với protein trong axit, bước sóng nền chuyển sang 595 nm. Khi đó, thuốc nhuộm chuyển sang màu xanh lam sáng.
Protein kết hợp với màu xanh lam của Coomassie trong 2 phút. Còn phức hợp protein-thuốc nhuộm với cấu trúc ổn định trong một giờ. Mặc dù các phép đo độ hấp thụ được thực hiện khuyến cáo trong 5 – 20 phút ngay khi phản ứng bắt đầu. Nồng độ protein trong xét nghiệm Bradford có thể được đo bằng máy phổ. Xét nghiệm Bradford được phát triển vào năm 1975 bởi Marion M. Bradford. Đồng thời, cho phép định lượng protein nhanh chóng và chính xác hơn so với quy trình Lowry hay xét nghiệm biuret. Đồng thời, phương pháp xét nghiệm này không dễ bị nhiễu bởi một số phân tử không phải protein. Chẳng hạn như ethanol, natri clorua hoặc magie clorua. Tuy nhiên, nó lại dễ bị ảnh hưởng bởi chất đệm kiềm mạnh. Điển hình là natri dodecyl sulfat (SDS).
5.5 Các phương pháp thấm và probe các đại phân tử
-
Phương pháp thấm Southern
Phương pháp thấm Southern được đặt tên theo người nghiên cứu – nhà sinh vật học Edwin Southern. Phương pháp này giúp probe, thăm dò sự hiện diện của chuỗi ADN trong mẫu hỗn hợp ADN. Các mẫu ADN trước hoặc sau khi cắt bằng enzym giới hạn được phân tách bằng phương pháp điện di trên gel. Tiếp đó, được chuyển đến màng lọc thấm nhờ hiện tượng mao dẫn. Màng lọc tiếp xúc với đầu dò ADN được đánh dấu. Chúng mang trình tự gen có thể lai ghép với đoạn ADN nhờ nguyên tắc bổ sung.
Tuy nhiên, phương pháp này ít được sử dụng do các kỹ thuật khác ưu việt hơn. Điển hình là PCR giúp phát hiện trình tự ADN cụ thể từ các mẫu ADN. Tuy nhiên, nó vẫn được sử dụng trong một số ứng dụng. Ví dụ như đo số bản sao gen biến đổi ở chuột biến đổi gen. Hoặc trong kỹ thuật tạo dòng tế bào gốc phôi nhờ gen knockout.
-
Phương pháp thấm Northern
Phương pháp thấm Northern giúp phát hiện sự hiện diện của phân tử ARN cụ thể. Từ đó, có thể so sánh tương đối giữa các mẫu ARN. Nó là sự kết hợp giữa phương pháp điện di trên gel của ARN biến tính với phương pháp thấm. ARN được phân tách dựa trên kích thước và chuyển đến màng lọc. Nó được thực hiện trước khi thăm dò nhờ nguyên tắc bổ sung với trình tự quan tâm đã được xác định. Tùy thuộc vào chất đánh dấu mà đưa ra kết quả riêng. Thế nhưng, hầu hết kết quả thể hiện là các dải đại diện cho kích thước ARN trong mẫu. Cường độ của nó liên quan đến số lượng dải ARN mục tiêu trong mẫu.
Nó thường được ứng dụng trong nghiên cứu thời điểm và mức độ biểu hiện gen. Mức độ thể hiện thông qua lượng ARN hiện diện trong các mẫu khác nhau nếu quá trình điều hòa không xảy ra sau phiên mã. Đồng thời, mức ARN thông tin phản ánh tỷ lệ protein tương ứng được sản xuất. Đây là công cụ hữu ích hàng đầu để xác định thời điểm và điều kiện gen trong mô sống.
-
Phương pháp thấm Western
Phương pháp thấm Western là kỹ thuật sử dụng protein cụ thể được tìm thấy từ một hỗn hợp protein. Nó giúp xác định kích thước của protein cô lập và định lượng biểu hiện của chúng. Trong phương pháp thấm Western, các protein lần đầu tiên được phân tách dựa vào kích thước trong lớp gel mỏng kẹp giữa hai tấm thủy tinh. Nó được gọi là SDS-PAGE. Sau đó, chúng được chuyển sang màng polyvinylidene fluoride (PVDF), nitrocellulose, nylon,… Màng lọc này có thể được thăm dò bằng dung dịch kháng thể.
Kháng thể liên kết với protein quan tâm rồi được hình dung bởi nhiều kỹ thuật khác nhau. Cụ thể là các phẩm màu, chất phát quang hóa học hay phóng xạ tự chụp. Thường kháng thể được các enzyme đánh dấu. Chất nền phát quang hóa học tiếp xúc với enzyme giúp phát hiện tổ hợp. Nó còn cho phép phân tích định lượng. Các phương pháp tương tự có thể được sử dụng để nhuộm trực tiếp protein cụ thể trong tế bào sống hoặc mô.
-
Phương pháp thấm Eastern
Phương pháp thấm Eastern giúp xác định các biến đổi sau quá trình protein dịch mã. Với kỹ thuật này, protein thấm trên màng PVDF hoặc nitrocellulose cùng chất nền giúp tìm hiểu các sửa đổi của protein sau dịch mã.
5.6 Kỹ thuật ADN microarray
Một ADN microarray (ADN chip) bao gồm các điểm được gắn với giá đỡ vững chắc như kính hiển vi. Mỗi điểm chứa một hoặc nhiều đoạn oligonucleotide ADN sợi đơn. Các dãy hay array chứa lượng lớn các điểm nhỏ trên một mặt kính duy nhất. Mỗi điểm có một phân tử đoạn ADN bổ sung cho chuỗi ADN đơn. Biến thể của kỹ thuật này cho phép biểu hiện gen trong một giai đoạn cụ thể. ARN trong mô được phân lập và biến chuyển thành ADN bổ sung (cADN) đánh dấu. cADN này sẽ lai các đoạn trên dãy. Nhiều dãy được tạo thành bởi các đoạn giống nhau. Điều này rất quan trọng trong so sánh biểu hiện gen của hai mô khác nhau. Điển hình là mô khỏe mạnh và mô ung thư.
Chưa kể, có thể đo gen nào được biểu hiện. Và nó thay đổi như thế vào cũng như các yếu tố khác. Có đa dạng cách để chế tạo các dãy. Trong đó, phổ biến nhất là chip silicon, các lam kính hiển vi với đường kính 100 micromet, các dãy được tinh chỉnh và dãy với các điểm lớn trên bề mặt tấm màng nhiều lỗ (macroarrays). Số lượng từ 100 đến 10,000 điểm trên một dãy nhất định. Ngoài ra, nó cũng được tạo từ phân tử khác ngoài ADN.
5.7 Oligonucleotide đặc hiệu alen
Oligonucleotide đặc hiệu alen cho phép phát hiện đột biến cơ sở đơn lẻ. Mà không cần dùng kỹ thuật PCR hoặc điện di trên gel. Mẫu dò ngắn đánh dấu cho tiếp xúc với ADN mục tiêu không phân mảnh. Quá trình lai có độ đặc hiệu cao do chiều dài đầu dò ngắn. Bởi vậy, sự thay đổi nhỏ của base đơn lẻ cũng khiến quá trình lai gặp nhiều khó khăn. ADN mục tiêu được rửa sạch để loại bỏ mẫu đánh dấu không lai. Sau đó, được phân tích để xác định sự hiện diện của mẫu dò bằng phóng xạ hoặc huỳnh quang. Trong thí nghiệm này, một nhóm kiểm soát được sử dụng để chắc chắn kết quả thành công.
Trong sinh học phân tử, quy trình công nghệ được phát triển liên tục. Đồng thời, loại bỏ các công nghệ cũ. Trước khi kỹ thuật điện di trên gel xuất hiện, kích thước phân tử ADN được xác định bằng tốc độ lắng trong gradient đường sucroza. Quá trình này tốn nhiều thời gian, công sức và chi phí thiết bị. Máy đo độ nhớt giúp đo kích thước phân tử ADN. Việc hiểu biết kỹ thuật cũ rất quan trọng bởi nó giúp giải quyết các vấn đề mà công nghệ mới không hỗ trợ được.
6. Mối quan hệ phức tạp của gen và protein
Gen và protein đóng vai trò quan trọng trong nghiên cứu sinh học phân tử. Gen là các đoạn thông tin trong axit nucleic lớn. Còn protein được coi là chất xúc tác, động cơ của quá trình sinh học. Sự tương tác và mối quan hệ giữa chúng giúp xác định và hiểu hơn về con đường sinh học đang được nghiên cứu. Protein có thể:
- Điều tiết và tác động lẫn nhau
- Đáp lại tín hiệu từ gen
- Đáp ứng tín hiệu từ bên ngoài tế bào
Chuỗi tương tác phức tạp này đang là trọng tâm nghiên cứu của nhiều nhà sinh học phân tử. Mỗi bước trong quá trình hoạt động của phân tử có thể bị ảnh hưởng bởi bệnh tật hoặc là mục tiêu của các loại thuốc. Hiểu rõ vai trò của từng phân tử này rất cần thiết để khám phá sâu hơn về sinh vật sống, cấu trúc phân tử. Đồng thời, hỗ trợ các nhà khoa học điều chỉnh quá trình sinh học. Bao gồm cả những nhà thiết kế thuốc và kỹ sư di truyền.
7. Xét nghiệm sinh học phân tử là gì?
Xét nghiệm sinh học phân tử đánh giá các chỉ thị sinh học ở mức độ phân tử. Chẳng hạn như các đoạn acid nucleic, gen hoàn chỉnh và bộ gen vi sinh vật. Nó bao gồm quá trình tổng hợp chuỗi gen PCR và mang đến bước tiến lớn trong nhận dạng và giải trình gen. Mục tiêu của kỹ thuật này là cung cấp thông tin nhanh chóng và chính xác về tác nhân gây bệnh và cải thiện quá trình điều trị. Có thể nói, xét nghiệm sinh học phân tử tạo nên bước nhảy vọt cho nền y học hiện đại.
Xét nghiệm sinh học phân tử bắt buộc đòi hỏi sử dụng cả chứng dương và chứng âm. Chứng dương là mẫu chứng chứa đoạn ADN/ARN mục tiêu đã biết trước. Còn chứng âm không chứa đoạn ADN/ARN mục tiêu. Điều này giúp kiểm soát quá trình nhiễm chéo và đảm bảo tính chính xác của phản ứng xét nghiệm.
8. Ứng dụng xét nghiệm sinh học phân tử trong chẩn đoán HBV và HIV
8.1 Xét nghiệm sinh học phân tử ở HBV
Xét nghiệm sinh học phân tử ở HBV là gì?
Xét nghiệm sinh học phân tử được ứng dụng trong chẩn đoán HBV, đo tải lượng hệ thống tự động. Nó giúp nhận diện vi khuẩn HBV, xác định lượng virus trước khi điều trị. Nhờ đó, có thể theo dõi được lượng virus trong suốt quá trình điều trị. Đồng thời, đánh giá được sự biến động để có liệu pháp điều trị cụ thể.
- Bệnh phẩm sử dụng: 4ml máu chống đông EDTA. Hoặc 1,2ml huyết tương người bệnh.
- Kết quả xét nghiệm có sau 3 ngày.
HBV đo tải lượng Real-time PCR
HBV đo tải lượng Real-time PCR tương tự như kỹ thuật xét nghiệm PCR. Tuy nhiên, có thêm thiết bị tính toán về mốc thời gian xảy ra phản ứng PCR. Nhờ đó, có thể xác định được số lượng và nồng độ mẫu thử ở giai đoạn này. Kết quả chẩn đoán tình trạng giai đoạn bệnh và sự phát triển của yếu tố gây bệnh chính xác hơn. Nó có vai trò đặc biệt quan trọng trong điều trị.
Một số kỹ thuật khác
Bên cạnh đó, để đảm bảo kết quả chính xác cần sử dụng một số kỹ thuật sau:
- Định tính HBV bằng kỹ thuật PCR: Phát hiện DNA của HBV trong máu hoặc trong tế bào gan kể cả khi HBsAg biến mất. Phương pháp này có độ nhạy và đặc hiệu cao.
- Xác định kiểu gen HBV bằng kỹ thuật giải trình tự hoặc RFLP: HBV có 8 kiểu gen khác nhau. Trong đó, genotype liên quan nhiều đến tiến triển bệnh, sự kháng thuốc và đột biến. Nghiên cứu lâm sàng cho thấy genotype C đáp ứng kém thuốc kháng virus. Tuy nhiên, nguy cơ đột biến và ung thư cao hơn genotype B. Bởi vậy, việc xác định kiểu gen có vai trò quan trọng trong chẩn đoán, điều trị và tiên lượng bệnh.
- Xét nghiệm sinh học phân tử tham gia xác định khả năng kháng thuốc của bệnh nhân viêm gan B mạn tính.
Tương tự như xét nghiệm sinh học phân tử ở HBV. Với HCV, nhà nghiên cứu tiến hành định tính bằng nhiều phương pháp. Điển hình là kỹ thuật PCR, đo tải lượng virus HCV và xác định kiểu gen HCV.
8.2 Xét nghiệm sinh học phân tử ở HIV
Giống như xác định HBV, trong quá trình chẩn đoán HIV, kỹ thuật sinh học phân tử được sử dụng để đo lượng virus HIV trong cơ thể. Nó được thực hiện thông qua việc sử dụng hệ thống tự động để đo tải lượng virus. Từ đó, đưa ra kết quả xét nghiệm chính xác. Xét nghiệm sinh học phân tử không chỉ giúp xác định số lượng virus HIV hiện có. Nó còn hỗ trợ nghiên cứu liệu pháp điều trị tối ưu và tiên lượng bệnh hiệu quả.
- Bệnh phẩm sử dụng: 4ml máu chống đông EDTA hoặc 1,5ml huyết thương.
- Kết quả xét nghiệm có sau 1 tuần.
Thực tế lâm sàng tồn tại nhiều loại vi sinh gây bệnh. Đặc biệt là các chủng mới như HIV, HCV, SARS và nhiều loại nấm khác. Khi đó, các phương pháp xét nghiệm vi sinh thông thường không đủ để xác định và đưa ra kết quả chẩn đoán chính xác. Trong trường hợp này, phương pháp xét nghiệm sinh học phân tử là công cụ cần thiết giúp chẩn đoán nhanh chóng, chính xác và hiệu quả. Chẳng hạn, để chẩn đoán viêm gan virus C, các bệnh lý do nấm chlamydia, adenovirus, dengue virus, người ta thường áp dụng các kỹ thuật tổng hợp PCR và Real-time PCR. Nó giúp cung cấp thông tin chính xác và quan trọng trong điều trị và quản lý bệnh.
Xem thêm:
- ADN tái tổ hợp là gì? Đột phá trong khoa học di truyền
- Công nghệ tế bào – Bước tiến nhảy vọt, ứng dụng mọi lĩnh vực
9. Hạn chế của xét nghiệm
Dưới đây là một số hạn chế của kỹ thuật xét nghiệm sinh học phân tử:
- Mẫu chuẩn và mẫu thử có thể không chính xác với mọi nồng độ. Nó chỉ trong phạm vị nồng độ nhất định. Bởi vậy, kết quả xét nghiệm trong một số trường hợp có thể không chính xác.
- Không phải vi sinh vật nào cũng được xác định bằng kỹ thuật sinh học phân tử. Bởi số lượng bản “giải trình tự gen” của vi sinh vật có giới hạn.
- Với Real-time PCR cũng điều kiện xét nghiệm nghiêm ngặt, mẫu chẩn cần tốt để so sánh với mẫu thử. Trong đó, cần so sánh một mẫu thử với 5 mẫu thật để hạn chế tối đa các sai sót có thể xảy ra.
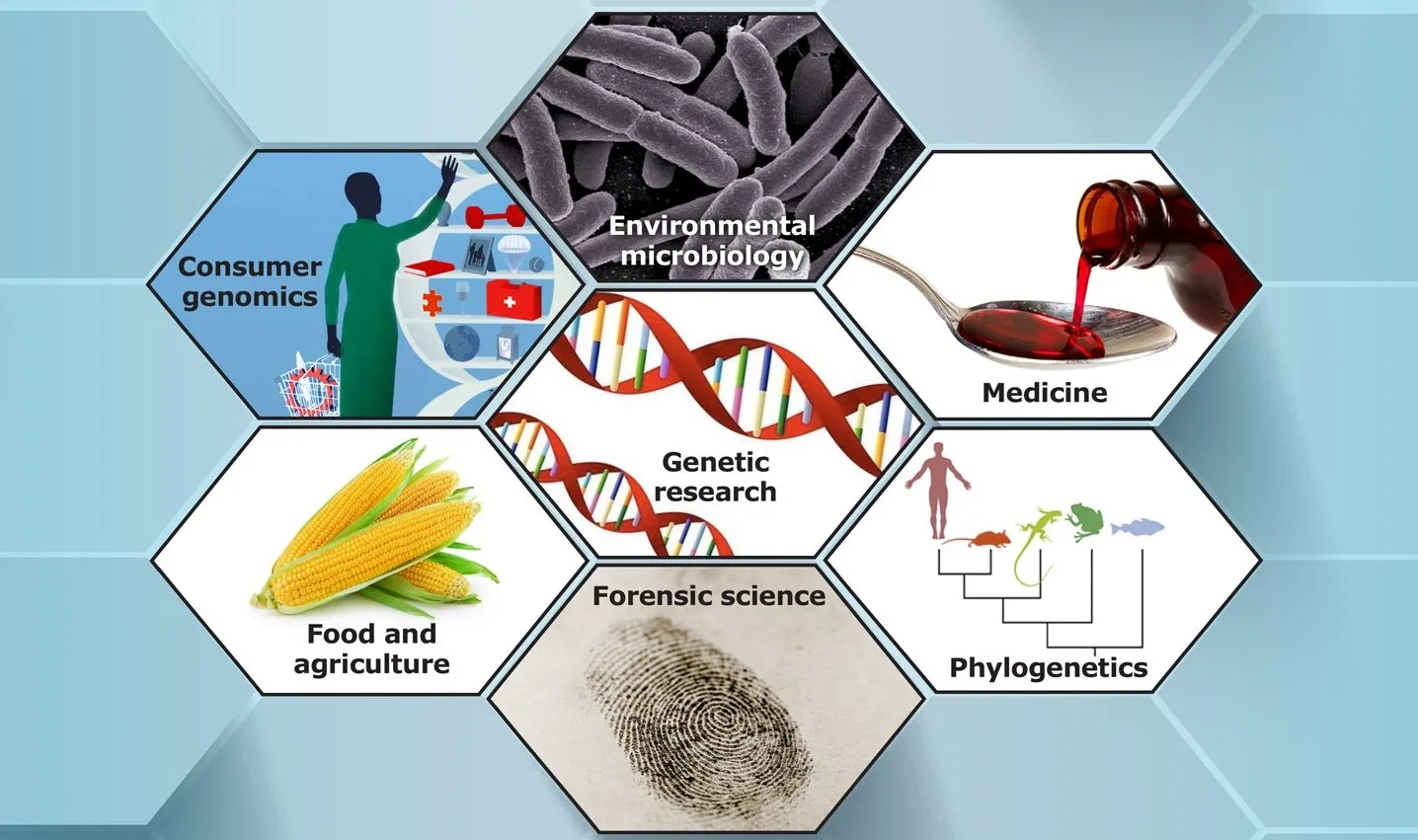
10. Ứng dụng của kỹ thuật sinh học phân tử
Xét nghiệm sinh học phân tử ra đời giúp giải quyết các vấn đề mà phương pháp truyền thống chưa thể làm được. Cụ thể:
- Thực hiện xét nghiệm chẩn đoán Covid-19, cúm A/H1N1, HPV,… Xét nghiệm kỹ thuật sinh học phân tử cho phép phát hiện và chẩn đoán bệnh lý nhanh chóng hơn, chính xác và hiệu quả.
- Real-time PCR hỗ trợ định lượng nồng độ tác nhân gây bệnh. Đây là yếu tố quan trọng giúp điều trị một số bệnh lý như HIV, viêm gan B, viêm gan C,…
- Khảo sát trên đa dạng mẫu bệnh phẩm như nước bọt, nước tiểu, dịch hô hấp, dịch màng bụng, phân, nước tiểu,…
- Hỗ trợ nghiên cứu cơ chế phát sinh bệnh lý hiệu quả trong y học.
- Ứng dụng và phát triển trong chẩn đoán thai kỳ trước và sau sinh.
11. Tạm kết
Xét nghiệm sinh học phân tử yêu cầu nghiêm ngặt về trang thiết bị và kỹ năng của người thực hiện. Đồng thời, đòi hỏi trình độ chuyên môn cao. Điều này đồng nghĩa với chi phí xét nghiệm tăng cao. Do đó, việc chỉ định xét nghiệm sinh học phân tử chỉ nên được thực hiện khi các phương pháp xét nghiệm truyền thống không đủ để đưa ra một chẩn đoán chính xác. Khi cần thực hiện xét nghiệm này, cần lưu tiên lựa chọn các trung tâm y tế và cơ sở uy tín, đảm bảo chất lượng. BCC chuyên cập nhật nhanh chóng và chính xác nhất các thông tin liên quan đến nghiên cứu và ứng dụng Công nghệ sinh học trong mọi lĩnh vực.